EBV R-GENE®
Kit PCR real-time per il rilevamento e la quantificazione accurati del DNA del virus di Epstein-Barr (EBV)
- Quantificazione accurata della carica virale di EBV su un ampio range lineare*
- Il kit è pronto all’uso e include i controlli interni e gli standard di quantificazione
- CE-IVD su diversi tipi di campioni e su tutte le principali piattaforme di estrazione e i sistemi PCR real-time
Maggiori informazioni
Vantaggi di EBV R-GENE®
Il virus di Epstein-Barr (EBV), conosciuto come l’agente eziologico della mononucleosi infettiva, è responsabile della linfoproliferazione delle cellule B (malattia linfoproliferativa post-trapianto - PTLD, linfoma di Burkitt, linfoma di Hodgkin ecc.) una complicanza grave per i pazienti immunocompromessi. Il monitoraggio ottimale dell’EBV è determinante per garantire la miglior gestione del paziente. EBV-R-GENE® consente la rilevazione rapida e specifica della carica virale anche prima della presenza di sintomi clinici ed è pertanto la soluzione ideale. Può contribuire a migliorare le opzioni di trattamento, misurarne l’efficacia del trattamento e monitorare eventuali ricadute. Per un monitoraggio più completo del paziente, l’ampia gamma R-GENE® permette di quantificare diversi virus in uno stesso campione e, naturalmente, di analizzare contemporaneamente diversi campioni per uno o più virus.
- Sensibile e riproducibile
- Misurazione affidabile dell’infezione da EBV
- Ampio range lineare
- Standardizzato
- Processazione uniforme con la gamma di prodotti R-GENE® (CMV R-GENE®, HSV1 HSV2 VZV R-GENE®, CMV HHV6,7,8 R-GENE®, BK Virus R-GENE®, Adenovirus R-GENE®, Parvovirus B19 R-GENE®) Profili di test armonizzati per analisi multiple in un solo ciclo
- Protocollo per convertire i risultati di quantificazione in UI/mL sulla base del primo Standard internazionale OMS
- Flessibile
- Convalidato per l’uso con vari tipi di campioni
- Uso con preparazione del campione manuale o automatica come NucliSENS® easyMAG® e tecnica di preparazione dell’analisi come il sistema di gestione dei liquidi easySTREAM™
- Validato per le principali piattaforme di PCR real-time
Tutto il necessario in un solo kit
Il kit pronto all’uso EBV R-GENE® misura la carica virale di EBV negli estratti di DNA di diversi campioni clinici. Questa analisi in PCR real-time con sonde a idrolisi basata sull’attività 5’ nucleasica della DNA Polimerasi amplifica una regione specifica del genoma di EBV consentendo sia il rilevamento qualitativo che la quantificazione.
- Quattro standard di quantificazione garantiscono una misurazione accurata della carica virale di EBV
- Un controllo di sensibilità convalida le prestazioni dell’analisi
- Un controllo interno (IC2) verifica il processo di estrazione, lisi compresa, e la presenza di inibitori dell’amplificazione nel campione
- Tutti i reagenti necessari ottimizzati per il rilevamento e la quantificazione di EBV per uso diagnostico in vitro sono pronti all’uso:
- Risparmio di tempo per i tecnici
- Riduzione del rischio di errore di manipolazione o diluizione
- Riduzione del rischio di contaminazione
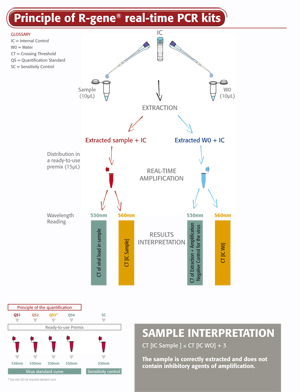
Procedura semplice
L’uso del kit EBV R-GENE® è semplice. È sufficiente aggiungere il campione di DNA estratto alla master mix PCR pronta all’uso e iniziare la reazione sul termociclatore PCR real-time appropriato, seguendo il programma ottimizzato di cicli termici descritto nelle “Istruzioni per l’uso”.
Clicca per ingrandire »
BIOMERIEUX, il logo blu, ARGENE®, R-GENE®, EASYMAG® e NUCLISENS® sono marchi utilizzati, depositati e/o registrati di proprietà di bioMérieux, o di una delle sue controllate o aziende. Qualsiasi altro nome o marchio è di proprietà dei rispettivi titolari.
Any other name or trademark is the property of its respective owner. - See more at: http://clinical.biomerieux.net/cmv-R-GENE-0#sthash.YR9WVorN.dpuf
| EBV R-GENE® (69-002B) | |
|---|---|
| Principio del test | Rilevamento e quantificazione del genoma di EBV |
| Informazioni per l’ordinazion | Codice 69-002B: EBV R-GENE® kit di quantificazione Disponibile anche con il codice 69-002: EBV R-GENE® Kit di quantificazione COMPLETO (include 69-002B Kit di quantificazione e kit di estrazione DNA cod. 67-000) |
| Tecnologia | PCR real-time / tecnologia Taqman 5’ nucleasi |
| Target genico | Gene BXLF1 che codifica per la timidina chinasi |
| Campione* | Sangue intero, plasma, LCS, biopsie, BAL |
| Limite di rilevazione | 4 copie/ PCR |
| Range dinamico di quantificazione | Fino a 5 106 copie/mL |
| Controlli inclusi | Controllo di estrazione + inibizione, controllo di sensibilità, controllo negativo |
| Risultati in | 75 minuti (passaggio di estrazione escluso) |
| Unità di riferimento | Copie/mL o conversione in UI/mL sulla base del primo Standard internazionale |
| OMS | |
| Numero di test | 90 test |
| Condizioni di conservazione | -18°C/-22°C per codice 69-002B (kit di quantificazione), +2°C/+8°C per codice 67-000 (kit di estrazione DNA) |
| Piattaforma di estrazione* automatica manuale validata | QIAamp DNA Blood Mini kit NucliSENS® easyMAG® MagNA Pure Compact MagNA Pure LC QIAcube QIAsymphony SP m2000sp VERSANT kPCR Molecular System SP |
| Piattaforma di amplificazione validata* | Life Technologies (Applied Biosystems) LightCycler SmartCycler RotorGene VERSANT kPCR Molecular System AD Biorad DX Real-Time system Stratagene / Agilent |
| Stato | Per uso diagnostico in vitro |
* si prega di verificare
Informazioni chiave su EBV
Cos’è EBV?
Il virus di Epstein-Barr (EBV) è un virus onnipresente che infetta la maggior parte della popolazione umana. Dopo una prima infezione (trasmissione con la saliva), EBV rimane latente nelle cellule B e può riattivarsi periodicamente negli individui sani. Tale riattivazione si verifica con una replicazione di EBV nell’orofaringe e non mostra alcun segno clinico.
Quali sono i soggetti più a rischio?
EBV è un agente eziologico per diverse condizioni cliniche tra cui la mononucleosi infettiva e diverse patogenesi cancerose quali il linfoma di Burkitt, il linfoma di Hodgkin e il carcinoma nasofaringeo. Negli individui immunosoppressi, la proliferazione incontrollata di cellule B indotta da EBV può anche provocare la malattia linfoproliferativa post-trapianto (PTLD), che è una causa importante di morbilità e mortalità nei destinatari di trapianto d’organo solido e nei pazienti sottoposti a HSCT.
Quali sono i vantaggi dei test molecolari su EBV?
Le analisi basate su PCR real-time per EBV consentono il rilevamento rapido e specifico prima dell’apparire dei sintomi clinici per contribuire al miglioramento degli esiti. Ciò è particolarmente importante per i pazienti immunosoppressi che sono a rischio di conseguenze particolarmente gravi di infezione. La PCR real-time quantitativa su EBV può essere utilizzata per contribuire alla diagnosi precoce di PTLD, tracciare il corso della malattia e monitorare la risposta al trattamento.
EBV R-GENE® e il primo Standard internazionale OMS per il virus di Epstein-Barr (EBV)
Vuoi calcolare il fattore di conversione per esprimere i risultati del tuo EBV R-GENE® in UI/ml?
Scarica un protocollo di calcolo.
R-GENE®: PUBBLICAZIONI
- Evaluation of the Epstein-Barr virus R-GENE quantification kit in whole blood with different extraction methods and PCR platforms
Fafi-Kremer et al.
J Mol Diagn. 2008 Jan;10(1):78-84. Epub 2007 Dec 28
- Measurement of HSV1, CMV, HHV6 and EBV viral loads in 83 bronchoalveolar lavage (BAL) from lung transplant recipients.
Germi et al.
Unit of Virus Host Cell Interactions, Grenoble
ESCV 2011
- Evaluation de la trousse EBV R-GENE (Argene) : Mesure de la charge virale EBV dans des prélèvements de sang total et dans les échantillons du panel européen QCMD
Brunet et al.
Service de virologie, Groupe Hospitalier Pitié-Salpêtrière, AP-HP, Paris
RICAI 2010
- Intérêt de la PCR quantitative EBV dans le suivi des greffés de moelle osseuse en pédiatrie
Billaud et al.
Laboratoire de Virologie, Hopital Debrousse, Lyon.
RICAI
- Comparative evaluation of the NucliSENS® easyMAG™ automated system for the extraction of viral DNA from whole blood samples: application to the monitoring of cytomegalovirus (CMV) and Epstein-Barr virus (EBV) loads
Pillet et al
Laboratoire de Bacteriologie-Virologie-Hygiène, Hopital Nord, CHU de Saint-Etienne, France.
ECCMID 2008
- Clinical and Laboratory Evaluation of the new Argene EBV DNA quantitative real-time PCR assay (R-GENE)
Laura Jane Scott et al
West Scotland Specialist Virology Centre, Gartnavel General Hospital, Glasgow, Scotland.
International Symposium on molecular diagnostics, 2006