CMV R-GENE®
Kit PCR Real-time per il rilevamento e la quantificazione del DNA di citomegalovirus (CMV)
- Quantificazione accurata della carica virale di CMV su un ampio range lineare
- Kit pronto all’uso con controllo interno e standard di quantificazione
- CE-IVD su tutte le principali piattaforme di estrazione e i sistemi PCR real-time, nonché su diversi tipi di campioni
Maggiori informazioni
Vantaggi di CMV R-GENE®
Citomegalovirus (CMV) è una complicanza grave per i pazienti immunocompromessi. Ecco perché sono necessari un rilevamento e un monitoraggio ottimizzati dell’infezione da CMV. CMV-R-GENE® è la soluzione ideale, poiché offre un rilevamento rapido e specifico. Consente di rilevare l’infezione prima della comparsa dei sintomi clinici, migliorando le opzioni di gestione; testare i pazienti durante il trattamento per misurare l’efficacia della cura e dopo il trattamento per monitorare eventuali recidive. Inoltre, per una maggiore efficienza, l’ampia gamma R-GENE® consente di qualificare e/o quantificare diversi virus in un campione o di analizzare contemporaneamente diversi campioni per un virus.
- Sensibile e riproducibile
- Misurazione affidabile dell’infezione da CMV
- Ampio range lineare
- Standardizzato
- Processazione parallela con la gamma di prodotti R-GENE® (EBV R-GENE®, HSV1 HSV2 VZV R-GENE®, CMV HHV6,7,8 R-GENE®, BK Virus R-GENE®, Adenovirus R-GENE®, Parvovirus B19 R-GENE®)
- Profili di test armonizzati per analisi multiple in un solo ciclo
- Protocollo per convertire i risultati di quantificazione di campione ematico in UI/mL sulla base del primo Standard internazionale OMS
- Flessibile
- Convalidato per l’uso con vari tipi di campioni
- Preparazione del campione manuale o automatica con NUCLISENS® EASYMAG® e piattaforma di preparazione dell’analisi come il sistema per la gestione dei liquidi easySTREAM™
- Qualificato per le principali piattaforme per PCR real-time
Un solo kit con tutto il necessario
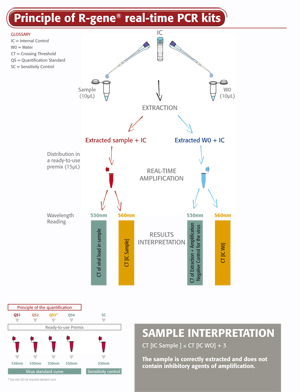
Il kit CMV R-GENE® è un kit di rilevamento molecolare pronto all’uso. Rileva e misura il genoma di CMV tramite PCR real-time dopo l’estrazione del DNA virale. Funziona con l’amplificazione e il simultaneo rilevamento di una regione specifica del genoma di CMV utilizzando la tecnologia Taqman 5’ nucleasi.
- Quattro standard di quantificazione garantiscono una misurazione accurata della carica virale di CMV
- Un controllo di sensibilità convalida le prestazioni dell’analisi
- Un controllo interno (IC2) verifica il processo di estrazione, lisi compresa, e la presenza di inibitori dell’amplificazione nel campione
- Include i reagenti necessari ottimizzati per il rilevamento e la quantificazione di CMV per uso diagnostico in vitro
Procedura semplice
L’utilizzo del kit CMV R-GENE® è semplice. Basta aggiungere il campione di DNA estratto alla master mix PCR pronta all’uso e iniziare la reazione sul termociclatore PCR real-time appropriato, seguendo il programma ottimizzato dei cicli descritto nelle “Istruzioni per l’uso”.
BIOMERIEUX, il logo blu, ARGENE®, R-GENE®, EASYMAG® e NUCLISENS® sono marchi utilizzati, depositati o registrati di proprietà di bioMérieux, o di una delle sue controllate o aziende.
Qualsiasi altro nome o marchio è di proprietà dei rispettivi titolari.
| CMV R-GENE® (69-003B) | |
|---|---|
| Principio del test | Rilevamento e quantificazione del genoma di CMV |
| Informazioni per l’ordinazione | Codice 69-003B: CMV R-GENE® kit di quantificazione Disponibile anche con il codice 69-003: CMV R-GENE® Kit di quantificazione COMPLETO (include 69-003B Kit di quantificazione e kit di estrazione DNA cod. 67-000) |
| Tecnologia | PCR real-time / tecnologia Taqman 5’ nucleasi |
| Target genico | proteina ppUL8 |
| Campione* | Sangue intero, plasma, siero, LCS, liquido amniotico, biopsie, urina, BAL |
| Limite di rilevamento | LoD 95% : 22 copie/PCR (555 copie/ mL) LoD 5%: 1 copia/PCR (30 copie/ mL) |
| Range dinamico di quantificazione | Fino a 107 copie/mL |
| Controlli inclusi | Controllo di estrazione + inibizione, controllo di sensibilità, controllo negativo |
| Risultati in | 75 minuti (passaggio di estrazione escluso) |
| Unità di riferimento | Copie/mL o conversione in UI/mL sulla base del primo Standard internazionale OMS |
| Numero di test | 90 test |
| Condizioni di conservazione | 18°C/-22°C per codice 69-003B (kit di quantificazione), +2°C/+8°C per codice 67-000 (kit di estrazione DNA) |
| Piattaforma di estrazione* automatica manuale validata | QIAamp DNA Blood Mini kit NUCLISENS® EASYMAG® MagNA Pure Compact MagNA Pure LC MagNA Pure 96 QIAcube QIAsymphony SP |
| m2000sp VERSANT kPCR Molecular System SP | |
| Piattaforma di amplificazione validata* | Life Technologies (Applied Biosystems) LightCycler RotorGene VERSANT kPCR Molecular System AD Biorad DX Real-Time system Stratagene / Agilent |
| Stato | Per uso diagnostico in vitro |
Informazioni chiave su CMV
Cos’è CMV?
Il citomegalovirus umano (HCMV) è un virus a DNA a doppio filamento della famiglia Herpesviridae. Dopo l’infezione primaria, che spesso si verifica nella prima infanzia, HCMV rimane in stato latente nell’ospite. Mentre i soggetti sani con CMV sono di norma asintomatici, HCMV può provocare infezioni secondarie ricorrenti in caso di immunosoppressione cronica o transitoria.
Quali sono i soggetti più a rischio?
L’infezione da HCMV è l’agente infettivo post-trapianto più comune dopo il trapianto di organo o il trapianto allogenico di midollo osseo. La febbre prolungata può essere l’unica manifestazione critica. Tuttavia, può comprendere diverse complicanze tra cui la polmonite interstiziale, una delle principali complicanze che si verifica in circa il 20% di tutti i destinatari dell’innesto e ha un tasso di mortalità del 90% senza trattamento. L’infezione da HCMV aggrava l’immunosoppressione, favorisce le superinfezioni ed è un fattore che scatena o accelera il rigetto o GVH (reazione trapianto contro ospite).
Mentre l’incidenza delle infezioni da HCMV nel corso dell’HIV/AIDS si è ridotta dell’80% con l’uso di trattamenti antri-retrovirali altamente attivi, i test sono sempre importanti per garantire il controllo di CMV e contribuire alla prevenzione delle infezioni opportunistiche correlate. Le manifestazioni cliniche dei pazienti con HIV/AIDS, più comunemente retinite e ulcera peptica, si verificano con un’alta immunosoppressione (linfociti T CD4+ inferiori a 50/mm3).
Durante la gravidanza, la comparsa di un’infezione materna primaria dà luogo a complicanze nel 50% dei casi di infezione fetale,che si rivela grave in circa il 10% dei casi, con danni neurologici.
Quali sono i vantaggi dei test su CMV?
Le analisi basate su PCR real-time per CMV consentono il rilevamento rapido e specifico prima della comparsa dei sintomi clinici per contribuire al miglioramento degli esiti, particolarmente importante nei casi di trapianto di organo/trapianto allogenico di midollo osseo e HIV/AIDS. I test aiutano a tenere traccia dell’efficacia del trattamento attivo e possono monitorare eventuali recidive dopo il trattamento.
CMV R-GENE® e il primo Standard internazionale OMS per il citomegalovirus umano
Vuoi calcolare il fattore di conversione per esprimere i risultati del tuo CMV R-GENE® in UI/ml? Scarica un protocollo di calcolo.
| Scarica il protocollol » | Scarica il file Excel » | Scarica il poster » |
Se desideri ordinare questo Standard internazionale OMS per CMV (codice 09-162). contatta il NIBSC al seguente link :
http://www.nibsc.org/products/biological_reference_materials/product_catalogue/detail_page.aspx?catid=09/162
Nota: I fattori di conversione presenti nel poster sono solo illustrativi per le combinazioni citate. bioMérieux raccomanda di determinare il fattore di conversione nel proprio laboratorio.
CMV R-GENE: PUBBLICAZIONI
- Cytomegalovirus load in inflamed intestinal tissue is predictive of resistance to immunosuppressive therapy in ulcerative colitis.
Roblin X, Pillet S, Oussalah A, Berthelot P, Del Tedesco E, Phelip JM, Chambonnière ML, Garraud O, Peyrin-Biroulet L, Pozzetto B. Am J Gastroenterol. 2011 Nov;106(11):2001-8. Epub 2011 Jul 26. - Cytomegalovirus infection in severe burn patients monitoring by real-time polymerase chain reaction: A prospective study
Bordes et al. Burns. 2011 May;37(3):434-9. Epub 2011 Jan 14. - Interêt de la recherche du cytomegalovirus par polymerase chain reaction dans le syndrome de Posner-Schlossman
Rodier-Bonifas et al. Journal français d'ophtalmologie, 2011 ; 34, 24-29 - Evaluation of new commercial real-time PCR quantification assay for prenatal diagnosis of cytomegalovirus congenital infection.
Ducroux A, Cherid S, Benachi A, Ville Y, Leruez-Ville M.J Clin Microbiol. 2008 Jun;46(6):2078-80. Epub 2008 Apr 16. - Multicentric evaluation of a new commercial cytomegalovirus (CMV) real-time PCR quantification assay
Gouarin S, Vabret A, Scieux C, Agbalika F, Cherot J, Mengelle C, Deback C, Petitjean J, Dina J, Freymuth F. J Virol Methods. 2007 Dec;146(1-2):147-54. Epub 2007 Jul 27. - Detection of cytomegalovirus (CMV) DNA in EDTA whole-blood samples: evaluation of the quantitative artus CMV LightCycler PCR kit in conjunction with automated sample preparation.
Michelin BD, Hadzisejdic I, Bozic M, Grahovac M, Hess M, Grahovac B, Marth E, Kessler HH. J Clin Microbiol. 2008 Apr;46(4):1241-5. Epub 2008 Feb 13.